Zrobiłem mały przegląd moich dotychczasowych tekstów i stwierdziłem, że jak dotąd dość po macoszemu potraktowałem elektrochemię. Postaram się w najbliższym czasie to nadrobić, bo jeszcze trafi na moją stronę jakiś kolega elektrochemik i się mocno zdenerwuje, że pomijam jego dziedzinę. A z ludźmi, którzy mają do dyspozycji różne elektrody kabelki i akumulatory, lepiej nie zadzierać. Tak na wszelki wypadek.
Analogie do wody
Najpierw trzeba zrobić małą powtórkę z zagadnień związanych z elektrycznością. Po pierwsze czym jest prąd elektryczny? W wielkim skrócie powiedzmy, że jest to uporządkowany ruch cząsteczek/cząstek obdarzonych ładunkiem elektrycznym, czyli w ciałach stałych elektronów, a w cieczach i gazach zwykle jonów. Prąd elektryczny charakteryzujemy poprzez podanie jego natężenia i napięcia elektrycznego. Natężenie (mierzone w amperach) wydaje się dość jasne do zrozumienia – im więcej nośników ładunku przemieszczających się w jednostce czasu tym większe natężenie.
A co z napięciem elektrycznym? Tu skorzystajmy z często przytaczanej analogii do wody. Zakładając takie samo natężenie przepływu, jaki strumień wody będzie miał większą energię – spływający z wysokości 3 metrów czy z 3 centymetrów? Odpowiedź jest oczywista, ale przełóżmy ją na kwestie prądu elektrycznego. Napięcie to różnica potencjałów, coś na kształt różnicy poziomów wody. Im większa różnica, tym większa energia jaką POTENCJALNIE mogą oddać nośniki ładunku, tj. elektrony lub jony.
Teraz pytanie ostatnie. Jak porównać, jaki strumień wody/ładunków elektrycznych ma większą moc użyteczną? Trzeba przy tym uwzględnić zarówno natężenie jak i napięcie (różnicę potencjałów). A więc moc to jest iloczyn napięcia i natężenia (czyli moc w watach uzyskamy mnożąc napięcie w woltach i natężenie w amperach).
[User:ARTE, via Wikimedia Commons]
O pożytkach z kupowania lodów
Z tej krótkiej wycieczki w rejony fizyki, wróćmy do naszej elektrochemii. Aby ją zrozumieć, kluczowe jest pojęcie potencjału elektrycznego w odniesieniu do różnych materiałów. Przede wszystkim rozważmy tu metale. Otóż każdy z nich zawiera elektrony, które są nośnikiem ładunku, a także każdy z atomów metalu może stać się jonem, kiedy utraci/odda jeden lub więcej elektronów. A jony to już jak pisałem, nośnik ładunku w cieczach, a więc w roztworach.
Zaobserwowano również, że atomy różnych pierwiastków, mają różny potencjał, czyli różną „skłonność” do oddawania elektronów i stawania się jonami. Jak u ludzi – jeden wystarczy, że zobaczy budkę z lodami i nie patrząc na cenę kupi od razu pięć gałek, a drugi będzie chomikował pieniądze i kupi lody tylko i wyłącznie, jak będzie wyprzedaż po złotówce za sztukę. Ponadto potencjał zależy od temperatury i tu nasza analogia z kupnem lodów również staje się użyteczna. Bo chętniej chyba kupimy lody przy czterdziestostopniowym upale niż podczas przymrozków?
Co ciekawe, potencjał elektryczny atomów danego pierwiastka nie jest w prosty sposób powiązany z jego masą, rozmiarem jądra atomowego czy innych jego właściwości fizycznych. Stanowi ich złożoną wypadkową i nie da się go łatwo przewidzieć czy wydedukować. Stąd trzeba po prostu na pamięć nauczyć się jaki potencjał ma dany atom. Pomaga w tym tzw. szereg napięciowy metali, czyli ich lista uszeregowana według potencjału elektrycznego.
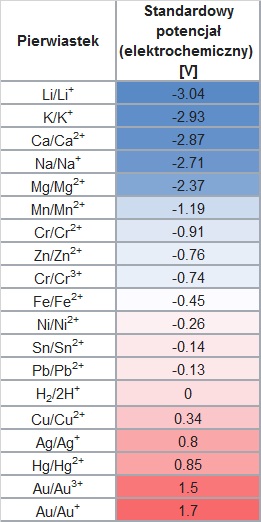
Ważne jest także to, że chemiczny potencjał elektryczny danego pierwiastka nie jest wartością wyznaczaną bezwzględnie, czyli określa się go w porównaniu do pewnego wzorca, czyli punktu odniesienia. Po długich bojach przyjęto wiele lat temu, że takim wzorcem będzie wodór i jego skłonność do oddawania elektronów. Ma on więc potencjał równy 0,0 V, co jednak nie znaczy, że nie oddaje on w ogóle elektronów. Wręcz przeciwnie, robi co całkiem chętnie.
Szereg napięciowy to potężne narzędzie w rękach elektrochemika, ale jak je można wykorzystać, opowiem już za tydzień 😉
Wojciech Smułek
